昆明理工大学余富朝教授团队在基于NH-取代烯胺酮的官能团化/环化反应方面取得了一系列进展,不仅开发了三种新合成方法,也实现了三类新化合物的合成和化合物库的构建,在有机合成和药物合成领域也都展现出了潜在的应用价值。相关工作发表在Organic Letters、Advanced Synthesis & Catalysis 和The Journal of Organic Chemistry杂志上,昆明理工大学生命科学与技术学院余富朝教授与陈丽老师、王保取老师和云南中医药大学王均亮博士为共同通讯作者,论文第一作者分别为昆明理工大学2023级硕士研究生魏远征、胡惠敏,2018级本科生谢芸花。
NH-取代烯胺酮,是一类最为常见的链状烯胺酮,结构中兼具多个亲核和亲电反应位点,具有结构多样、价廉易得等优势,是有机合成和药物开发的重要合成中间体,常用于合成具有潜在生物活性的杂环化合物和天然产物等。官能团化反应和串联环化反应是有机合成化学中两种步骤经济的合成策略,具有较高的原子经济性和合成效率。因此,基于简单易得的NH-取代烯胺酮为原料,发展新型的官能团化/环化反应,简洁高效构建结构多样的新化合物,具有重要的学术研究意义和实际应用价值。
进展一:二氢吡啶是一类重要的氮杂环化合物,广泛存在于许多药物、天然产物和有机合成中间体结构中。与已得到广泛研究的1,4-二氢吡啶相比,构建1,2-二氢吡啶的方法仍十分有限且具有挑战性,因此开发新合成方法来高效制备1,2-二氢吡啶是非常有必要的。近日,余富朝教授团队报道了一种铁(III)催化甲烷磺酸(MSA)介导的NH-取代烯胺酮和1,3-二氧杂环戊烷的三组分反应,在室温下合成了1,2-二氢吡啶。值得注意的是,这是第一个通过[3+2+1C]环化反应构建1,2-二氢吡啶的实例,该反应中的1,3-二氧杂环戊烷不仅是合成二氢吡啶的反应物也作为反应溶剂。(Org. Lett. 2025. DOI: 10.1021/acs.orglett.5c03165)

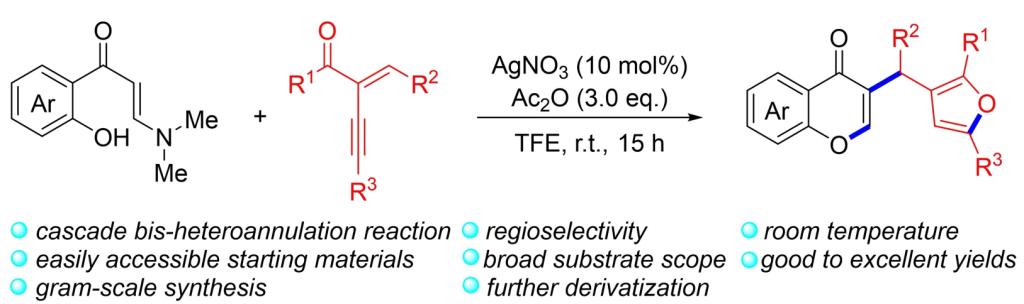
进展二:4-吡啶酮是天然产物和药物分子中最为常见的结构单元,具有广泛的药理活性。因此,4-吡啶酮骨架的合成方法已得到广泛研究。然而,这些合成方法仍存在着一些局限性,如使用复杂的功能化前体、苛刻的反应条件、反应效率低、使用过渡金属催化剂和繁琐的处理过程等。2025年,余富朝教授团队开发了一种基于NH-取代烯胺酮和重氮化合物的Wolff重排/[3+3]环化的新方法,高效合成结构多样的4-吡啶酮类化合物。该合成方法无需任何催化剂,以中等至优秀的产率合成具有广泛底物范围的4-吡啶酮,具有绿色的反应条件、宽泛的底物范围、克级合成和衍生化反应的实用性等特点。(Adv. Synth. Catal. 2025, 367, e202401561)

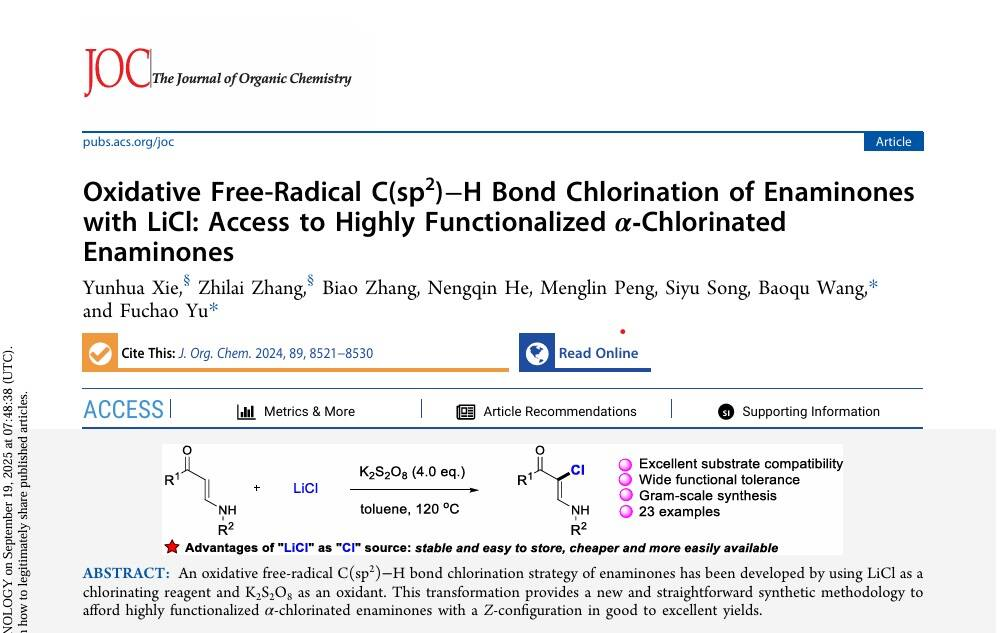
进展三:碳氯键(C-Cl)构建是有机合成化学的重要内容,其相关研究为天然产物合成、药物研发和功能材料等领域的发展作出了重要贡献。长期以来,双键上的C-Cl键构建主要利用两类氯源——有机氯化试剂和无机氯化试剂来实现。然而,有机氯化试剂存在着制备困难、价格昂贵等限制,而一些非盐类无机氯化试剂,如氯气、盐酸、三氯化磷等,则存在毒性大、储存困难、反应效率低等问题。氯化锂和氯化钠作为氯化试剂,在价格和来源等方面优势明显。2024年,余富朝教授团队开发了一种氧化自由基介导的C(sp²)-H键氯化策略,能够以易得的NH-取代烯胺酮类化合物和氯化锂为原料,高效构建具有Z-构型的α-氯代烯胺酮。该新方法的优势在于:1)采用廉价易得的氯化锂作为氯源,在无金属条件下实现氯化反应;2)具有优异的底物普适性和官能团兼容性;3)后处理简便、收率良好且可实现克级规模制备。(J. Org. Chem. 2024, 89, 8521−8530)
目前,研究团队正在开发这些产物和合成方法的深度应用,并进一步发展NH-取代烯胺酮的新型官能团化/环化反应研究,为天然产物、生物活性分子及功能性有机分子的合成和修饰提供方法学支持。
相关工作得到了国家自然科学基金项目、云南省自然科学基金和“兴滇英才支持计划”青年人才项目的资助。
(供稿:生科学院)
 滇公网安备53011402000430号 All Rights Reserved © Kunming University of Science and Technology
滇公网安备53011402000430号 All Rights Reserved © Kunming University of Science and Technology